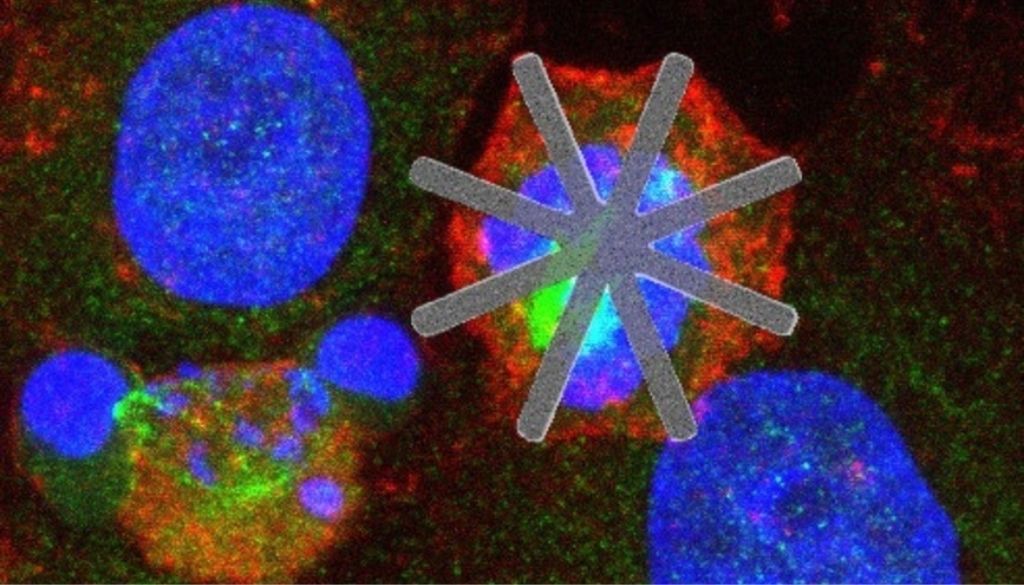
Investigadores del Instituto de Química Médica del Consejo Superior de Investigaciones Científicas (IQM-CSIC) han diseñado una plataforma universal de nanopartículas de óxido de hierro capaz de integrar, en un único paso, múltiples radioisótopos empleados en diagnóstico por imagen y en tratamientos oncológicos. El avance, publicado en la revista NPJ Imaging, supone un cambio relevante en el campo de la medicina nuclear y la radioteranóstica.
El desarrollo responde a una limitación histórica de los radiofármacos: la necesidad de utilizar estrategias químicas diferentes para cada radioisótopo. Tradicionalmente, estos compuestos combinan material radiactivo con moléculas biológicas que actúan como vehículos hacia los tejidos diana, lo que obliga a diseñar estructuras específicas para cada elemento. Este proceso no solo es complejo y costoso, sino que en algunos casos dificulta la viabilidad clínica.
La nueva tecnología del IQM-CSIC propone una solución basada en nanomateriales. Las nanopartículas de óxido de hierro permiten incorporar en su núcleo una amplia variedad de radiometales, manteniendo una elevada estabilidad en entornos biológicos. Según los resultados experimentales, el sistema alcanza retenciones superiores al 97 % incluso tras siete días en suero humano, un parámetro crítico para la seguridad y eficacia de los radiofármacos.
El estudio, liderado por el grupo de Nanomedicina, Imagen y Modelos 3D, contó con la participación de más de una decena de instituciones nacionales e internacionales, entre hospitales, centros de investigación y universidades. Los investigadores seleccionaron diez radiometales utilizados habitualmente en la práctica clínica y sintetizaron diez nanorradiofármacos distintos: tres orientados a PET, cuatro a SPECT y tres con aplicaciones terapéuticas.
Uno de los principales retos en la medicina nuclear es la unión estable entre el radioisótopo y el vehículo biológico. En la actualidad, este proceso suele depender del uso de quelantes, moléculas que actúan como “pinzas moleculares” para estabilizar los metales radiactivos. Sin embargo, la falta de quelantes universales limita la flexibilidad de los diseños farmacológicos. La plataforma desarrollada por el CSIC evita esta restricción al integrar directamente los isótopos en la estructura del nanomaterial.
Las pruebas realizadas en modelos animales confirmaron la versatilidad del sistema. Las nanopartículas mostraron capacidad para acumularse en tumores sólidos, incluyendo glioblastomas, lo que abre posibilidades tanto en diagnóstico como en radioterapia dirigida. Asimismo, demostraron utilidad en el marcaje de trombos, ampliando su potencial más allá de la oncología.
Otro hallazgo relevante fue el perfil de eliminación biológica. Los investigadores verificaron que las nanopartículas se excretan rápidamente por vía renal, reduciendo el riesgo de acumulación de radiactividad o de hierro en el organismo. Este comportamiento favorece la seguridad del paciente y posibilita la administración de terapias repetidas, un aspecto fundamental en enfoques teranósticos.
De acuerdo con los autores, la principal fortaleza del sistema radica en que conserva sus propiedades químicas y biológicas independientemente del radioisótopo incorporado. Este rasgo contrasta con los radiofármacos convencionales, que suelen requerir rediseños específicos para cada aplicación clínica.
El avance abre la puerta a una nueva generación de radiofármacos más simples de desarrollar, potencialmente más seguros y con amplias aplicaciones en diagnóstico precoz y tratamiento personalizado del cáncer, uno de los grandes objetivos de la medicina nuclear contemporánea.
No te pierdas una noticia, suscribete gratis para recibir DiarioSalud en tu correo, siguenos en Facebook, Instagram, Twitter, Linkedln, telegram y Youtube